Az ELKH Kísérleti Orvostudományi Kutatóintézet (KOKI) Katona István által vezetett Molekuláris Neurobiológia munkacsoportja és az ELKH Természettudományi Kutatóközpont (TTK) Keserű György által vezetett Gyógyszerkémia munkacsoportja egy új eljárást dolgozott ki, amelynek segítségével nanométeres pontossággal mérhető a gyógyszerek kötési helye az idegsejtek felületén. Az erről szóló publikáció a rangos Nature Communications szaklapban jelent meg.
Az idegrendszer különlegesen összetett felépítése hatalmas kihívást jelent a pszichiátriai betegségek megértésében és kezelésében. Az agy több mint 100 féle sejttípusában termelődő közel 20000 fehérje mennyisége és térbeli eloszlása idegrendszeri betegségekben jelentősen megváltozik. A molekuláris változások nyomon követése rendkívül nehéz, mert nanoskálájú mérettartományban (azaz a milliméter milliomodrészének tartományában) következnek be. Mivel a különböző idegsejttípusokban a változás iránya és mértéke is eltérő lehet, ezért az idegrendszeren ható gyógyszerek pontos sejttípus-specifikus kötődési mintázatának mérése kiemelten fontos a gyógyszerek hatásmechanizmusának és mellékhatásainak megértésében.
A KOKI és a TTK kutatói ezért közösen kidolgoztak egy új eljárást, amelyben fluoreszcens molekulák segítségével nanométeres pontossággal lehet farmakológiai méréseket végezni receptorokon, ioncsatornákon és enzimeken. Az új módszernek a FarmakoSTORM nevet adták, amely a STORM (SzTochasztikus Optikai Rekonstrukciós Mikroszkópia) szuperrezolúciós mikroszkópos eljáráson alapul. A FarmakoSTORM módszer segítségével a kutatók felfedezték, hogy a Richter Gedeon gyógyszergyár által fejlesztett, ipartörténeti jelentőségű cariprazine gyógyszer a Calleja-szigetek elnevezésű agyterületen található szemcsesejtekhez kötődik a legnagyobb mennyiségben. Ezeknek az idegsejteknek az élettani és kórélettani jelentőségéről eddig semmit nem lehetett tudni. A cariprazine az egyik legígéretesebb új gyógyszer a skizofrénia, a bipoláris betegség és a depresszió kezelésében, éves forgalma már meghaladja az 1 milliárd dollárt. Ezért a magyar kutatók felfedezése – a módszertani áttörés mellett – azért is kiemelkedően fontos, mert új utakat nyit a cariprazine hatásmechanizmusának és a pszichiátriai betegségek neurobiológiai alapjainak megértésében.
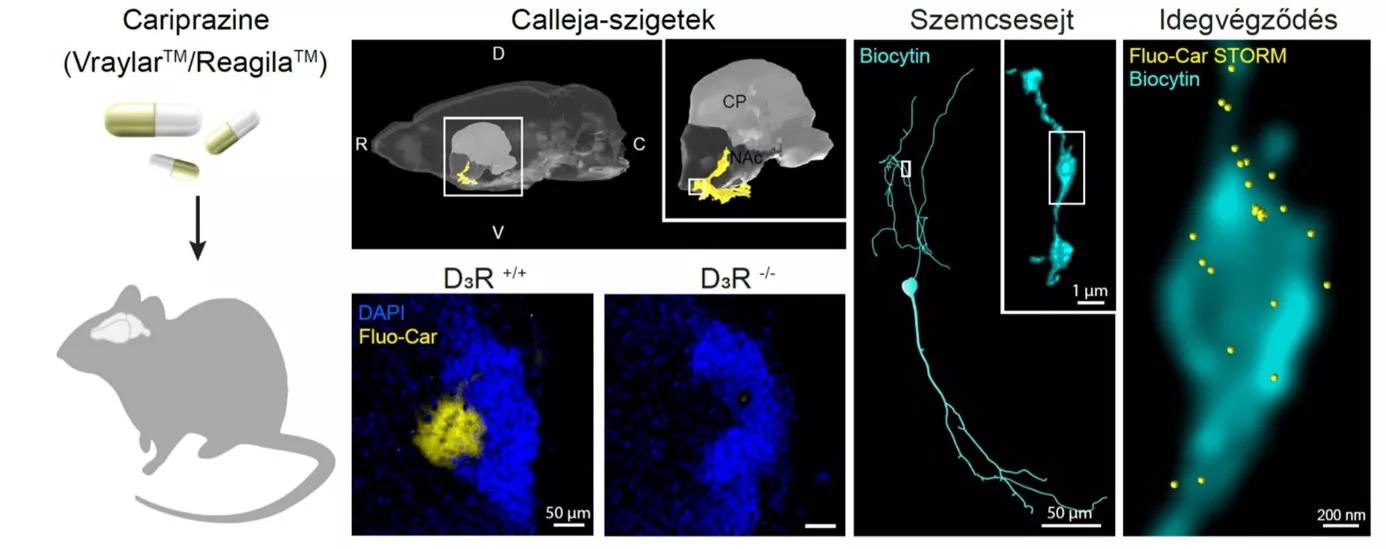
A cariprazine gyógyszer legnagyobb mennyiségben a Calleja-szigeteken található D3 dopamin receptorokhoz kapcsolódik. A Calleja-szigetek fő sejttípusa a szemcsesejt, amelynek idegvégződésein található a világító cariprazine molekulák kötőhelye. Ez a felfedezés arra utal, hogy a Calleja-szigetek szemcsesejtjei fontos szerepet játszanak a pszichiátriai betegségekben.
A Prokop Susanne és Ábrányi-Balogh Péter megosztott elsőszerzőségével készült tanulmány a Nature tudományos lapcsalád nyílt hozzáférésű (Open Access), magas nemzetközi presztízsű folyóiratában, a Nature Communications-ben jelent meg.
A kutatást többek között a Nemzeti Agykutatási Program, az NKFIH „Élvonal” pályázata, valamint a Semmelweis Egyetem EFOP-3.6.3-VEKOP-16-2017-00009 kódszámú programja támogatta.
Publikáció:
Prokop S., Ábrányi-Balogh P., Barti B., Vámosi M., Zöldi M., Barna L., Urbán G.M., Tóth D.A.,Dudok B., Egyed A., Deng H., Leggio G.M., Hunyady L., van der Stelt M.,Keserű G.M. és Katona I. (2021) PharmacoSTORM nanoscale pharmacology reveals cariprazine binding on Islands of Calleja granule cells. Nature Communications 12, 6505.