Egy nemzetközi együttműködés keretében sikerült áttörést elérni a COVID-19 egyik kulcsfehérjéje, a fő proteáz működésének gátlásában. Jóllehet a kutatások alig fél éve indultak, a konzorcium a molekuláris LEGO-koncepció alkalmazásával több mint 70 olyan molekulát talált, amelyek megfelelő kiindulópontul szolgálhatnak a gyógyszerfejlesztéshez.
Az ELKH Természettudományi Kutatóközpont (TTK) Gyógyszerkémiai Kutatócsoportja is részt vesz abban kutatási programban, amely az Oxfordi Egyetem, az angliai Diamond részecskegyorsító és az izraeli Weizmann intézet kutatócsoportjainak együttműködésével a SARS-Cov-2 koronavírus fehérjéinek gátlása révén kíván új lehetőségeket találni a COVID19 fertőzés kezelésére. A konzorcium eredményeit a Nature Communication folyóirat közli (https://www.nature.com/articles/s41467-020-18709-w), és az eredményeket a lap egy szerkesztőségi cikkben is méltatja (https://www.nature.com/articles/s41467-020-18710-3).
A kutatások a vírus fehérjéinek elkülönítésével és tisztításával kezdődtek, ennek eredményeképpen sikerült a vírus szaporodása szempontjából lényeges fehérjét, a fő proteázt azonosítani. Ez az enzim felel azoknak a vírus életképessége szempontjából fontos fehérjéknek a kialakításáért, amelyeket a vírus genetikai állománya kódol, ezért eredményes gátlása megakadályozza a vírus szaporodását. A terápiás lehetőségek szempontjából bíztató, hogy a vírus fő proteázának működése alapvetően eltér az emberi proteázokétól, így a kifejlesztett gátlószereknek várhatóan nem lesznek a proteáz gátlásából adódó veszélyes mellékhatásai.
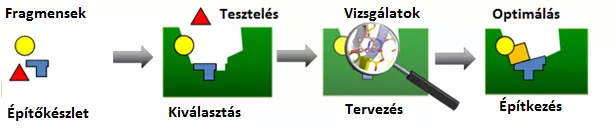
A kutatások az AIDS kezelésére irányuló vírus elleni gyógyszerek kifejlesztése során már sikerrel alkalmazott, szerkezetalapú gyógyszertervezés alapján indultak el, amelynek során elsőként meg kellett határozni a célfehérje háromdimenziós szerkezetét. Bár az első fehérjeszerkezetet német kutatók közölték le április 24-én a Science-ben (DOI: 10.1126/science.abb3405), a magyar kutatók részvételével dolgozó nemzetközi konzorcium ekkor már javában dolgozott a reményteli új molekulák azonosításán. Erre a célra a kutatók egy új, hatékony eljárást dolgoztak ki, amely a molekuláris LEGO-koncepción alapul, és a fehérjéhez kötődő, egyszerű molekuláris építőelemek, azaz fragmensek hatékony felismerését teszi lehetővé.
A megoldás egy lényeges eleme, hogy a magyar kutatócsoport által tervezett fragmensek nem csak megtalálják a fehérje alkalmas üregeit, de ott reakcióba is lépnek a fehérjével, így beleragadnak annak zsebeibe. Ezek a molekulák olyan erős és tartós kölcsönhatást alakítanak ki, amely megakadályozza a gyógyszermolekula távozását a kötőhelyről, és így a gátlás állandósul. A magyar, angol és izraeli kutatók által kifejlesztett molekulakészleteket az angol Diamond részecskegyorsítóban vizsgálták. A fehérje kristályait külön-külön 1250 különböző fragmens oldatába áztatták, majd röntgendiffrakciós módszerrel meghatározták, hogy a fehérjéhez kötődő 74 fragmens hogyan helyezkedik el a proteáz kötőzsebében.
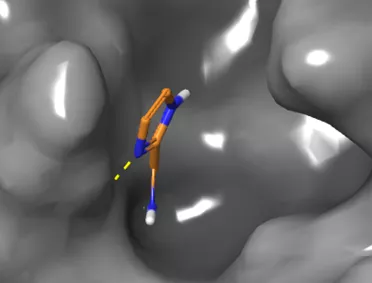
Az új eljárásnak és részecskegyorsítónak köszönhetően a méréseket kevesebb mint egy hónap alatt sikerült elvégezni. A vizsgálatok alapján a tesztelt magyar fejlesztésű reaktív fragmensek közül több is hatékonynak bizonyult, amelyek ígéretes kiindulópontul szolgálhatnak, és így hozzájárulhatnak új COVID-terápiák kifejlesztéséhez. A magyar építőelemek különlegessége, hogy további referenciafehérjék működését nem gátolták, így a mellékhatások lehetősége tovább csökken. Az magyar kutatócsoportban már folyik az ígéretes fragmensek továbbépítése, amit a Nemzeti Kutatási, Fejlesztési és Innovációs Hivatal mellett az Egyesült Királyság Külügyminisztériuma is támogat.
A molekuláris LEGO-koncepció
Már több mint száz éve annak, hogy Emil Fischer és Paul Erlich a molekulák és a szervezet fehérjéi között kialakuló molekuláris kölcsönhatásokra vezette vissza a gyógyszerek hatékonyságát. A fehérjék szerkezetéről szerzett ismeretek sokasodásával az is kiderült, hogy a gyógyszermolekulák azáltal fejtik ki hatásukat, hogy a fehérjék kisebb-nagyobb üregeibe kötődnek. Az ilyen üregek, valamint a bennük megfelelő kölcsönhatásokat kialakítani képes molekulák azonosítása a gyógyszerkutatás kezdeti szakaszának egyik legnagyobb kihívása. A múlt század végéig az üregekbe illeszkedő molekulákat a korábban más célra előállított molekulák közül próbálgatással igyekeztek kiválasztani. Egy új megközelítésnek köszönhetően az utóbbi tíz évben egy, a gyógyszereknél lényegesen kisebb méretű molekulák (fragmensek) tesztelésén és továbbépítésén alapuló molekuláris LEGO-módszer alapjait sikerült lerakni. A módszer szerint a ligandumok keresése a fragmensek kötődésének vizsgálatával indul, és azon a felismerésen alapul, hogy az ilyen molekulák nagyobb valószínűséggel kötődnek a fehérjék üregeihez, mint a nagyobb, gyógyszerjelölt-méretű molekulák. Ennek következménye, hogy már néhány száz, vagy néhány ezer fragmenst tartalmazó könyvtár szűrővizsgálata is kiindulópontul szolgáló találatot adhat. A kiindulópontoknak az üreg jellegzetességeit figyelembe vevő továbbépítése, vagy több találat esetén összekapcsolása új gyógyszerjelöltekhez vezethet.