A magyar kutatók által „fejlődési otthontalanság”-nak nevezett jelenséget az Eötvös Loránd Kutatási Hálózathoz tartozó Kísérleti Orvostudományi Kutatóintézet (ELKH KOKI) Katona István által vezetett Lendület Molekuláris Neurobiológia munkacsoportja ismerte fel, és igazolta jelentőségét a fejlődő idegrendszert érő magzatkárosító hatások kivédésében.
Sejtjeink többsége szoros molekuláris kapcsokkal összekötve a számára ideális szöveti mikrokörnyezetben működik. Ha egy hibás sejt kapcsolatait elveszíti és kiszakad a szöveti mikrokörnyezetéből, akkor beindul a programozott sejthalál speciális típusa, a görög szavak alapján képzett „anoikis”, ami „otthontalanságot” jelent. A folyamatosan osztódó őssejtek esetében az anoikis – azaz az otthontalanná válás – különösen fontos. Jól ismert tény, hogy a daganatos áttétek képződése során a tumorsejt „meg tud szökni” az anoikis folyamata elől. Nyitva maradt azonban az a kérdés, hogy azok az egészséges sejtek – mint például az egészséges idegsejtek –, amelyeknek osztódás után messzebbre kell vándorolniuk születési helyüktől, vajon hogyan kerülik el az anoikist? Ráadásul a fejlődő agyban kizárólag csillagászati számokkal jellemezhető a sejtosztódások száma, ezért elkerülhetetlenek a véletlenszerű, illetve a környezeti hatások, mint amilyenek például az anyai alkoholfogyasztás által kiváltott osztódási és vándorlási hibák.
Az ELKH KOKI kutatói azt feltételezték, hogy léteznie kell egy védekező mechanizmusnak a fejlődő agyban, amely megakadályozza, hogy az osztódó idegi őssejtek rossz helyre kerüljenek, és további osztódásukkal hibás sejtcsomók – úgynevezett heterotópiák –, vagy akár tumorok kialakulását okozzák. László Zsófia, a Semmelweis Egyetem doktorandusza, és Lele Zsolt, az ELKH KOKI kutatója kidolgozott egy egérmodellt, amelynek segítségével bizonyították a fejlődési anoikis jelenséget, és felfedezték, hogy a jelenség kulcsszereplője egy eddig ismeretleanoikin feladatú fehérje, az ABHD4 enzim. Sikerült azt is feltárniuk, hogy az ABHD4 által közvetített „fejlődési anoikis” nélkülözhetetlen az anyai alkoholfogyasztás hatására kialakuló sejthalálhoz az embriók agyában. Eredményük ezért a magzati alkohol szindrómával együtt járó „kisfejűség” jelenségének megértéséhez is jelentősen hozzájárul.
A László Zsófia és Lele Zsolt megosztott elsőszerzőségével megjelent tanulmány a hivatalos bírálói szerint „új koncepció a fejlődés-neurobiológiában”, és „új utakat nyit az idegsejtek keletkezésének kutatásában”.
A munka a Nature tudományos lapcsalád nyílt hozzáférésű (Open Access), nagy nemzetközi presztízsű folyóiratában, a Nature Communications-ban jelent meg.
Elérhetőség:
*László Z, *Lele Z, Zöldi M, Miczán V, Mógor F, Simon GM, Mackie K, Kacskovics I, Cravatt BF és Katona I (2020) ABHD4-mediated developmental anoikis safeguards the embryonic brain. Nature Communications, DOI: 10.1038/s41467-020-18175-4.
A kutatást többek között a Nemzeti Agykutatási Program, az NKFIH „Élvonal” pályázata, valamint a Semmelweis Egyetem EFOP-3.6.3-VEKOP-16-2017-00009 kódszámú programja támogatta.
Kapcsolat: Dr. Katona István, @email, mobilszám: +36 20 423 0651.
Képek
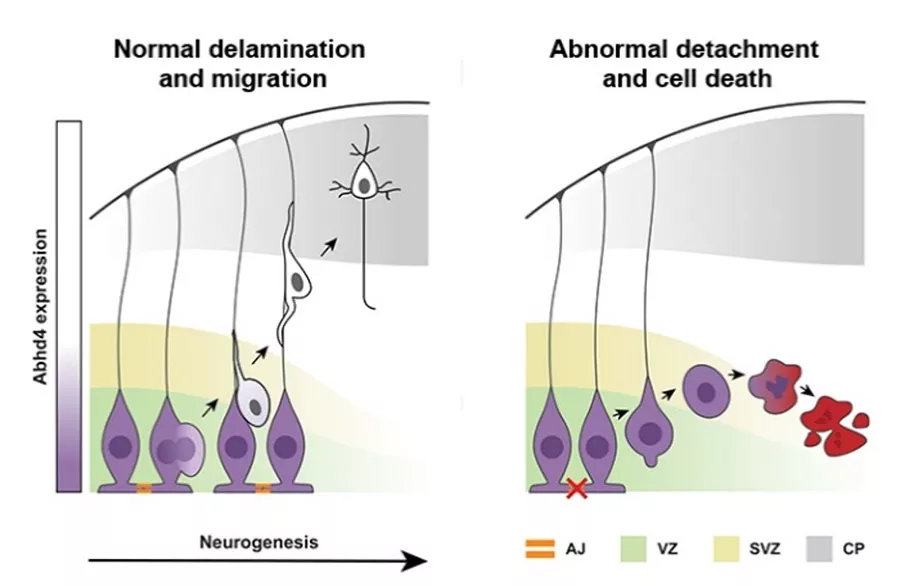
Az egészséges idegsejtek osztódás után felvándorolnak az agykéreg felső rétegeibe, miközben az ABHD4 enzim szintje lecsökken. A hibás sejtekben azonban az ABHD4 segítségével beindul az anoikis típusú sejthalál jelensége.
A kép készítője Balogh Kata
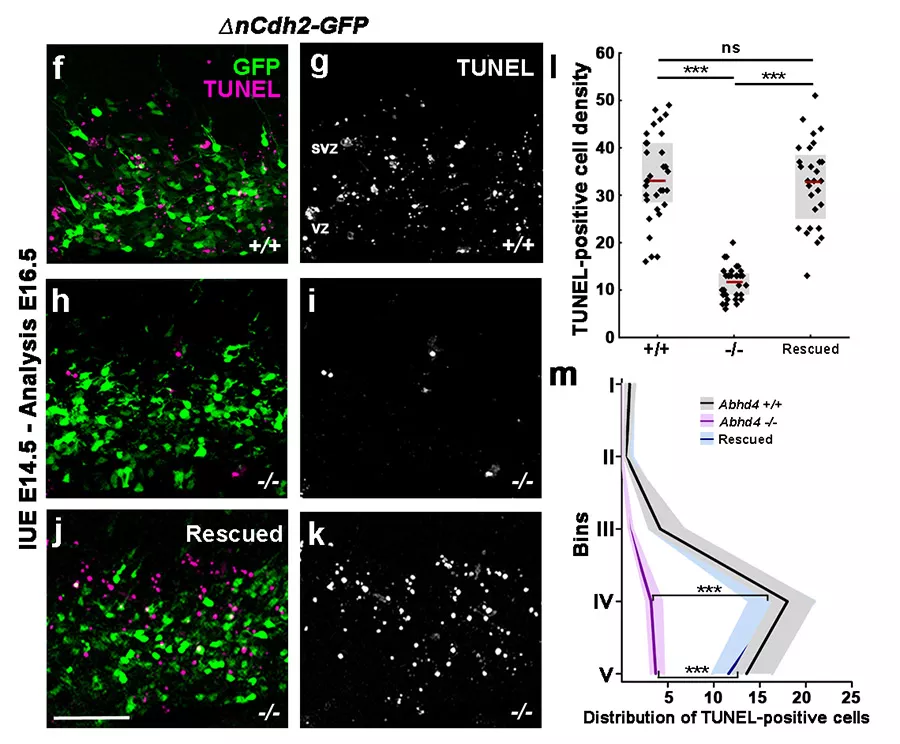
A domináns N-cadherin elektroporálása megnövekedett sejthalált okoz (f és g panel), ami az ABHD4 génkiütött állatokban nem jelentkezik (h és i panel). Az ABHD4 visszajuttatása a génkiütött állatokba helyreállítja a megnövekedett sejthalált.
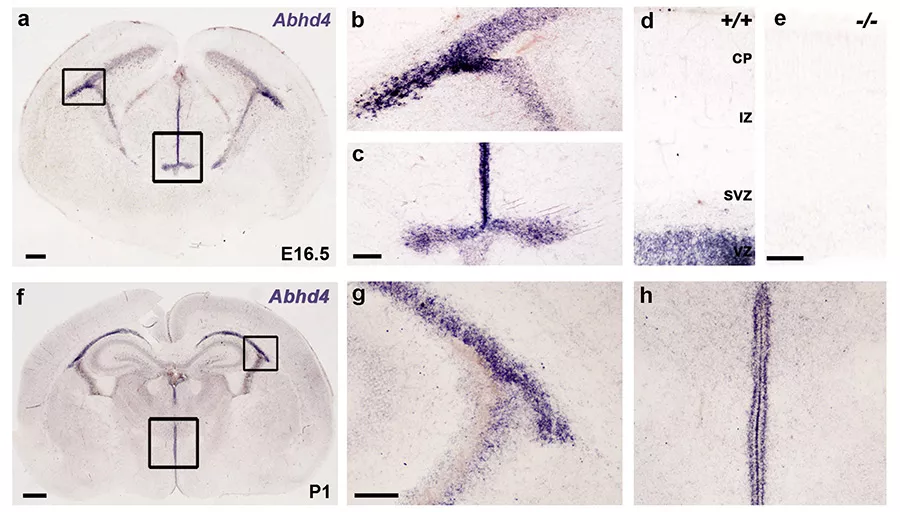
Az ABHD4 expressziója (lila színnel jelölve) az fejlődő agykéreg osztódó zónáiban. Az e. panelen, ami egy ABHD4 génkiütött állatból készült, látszik a jelölés specifikussága
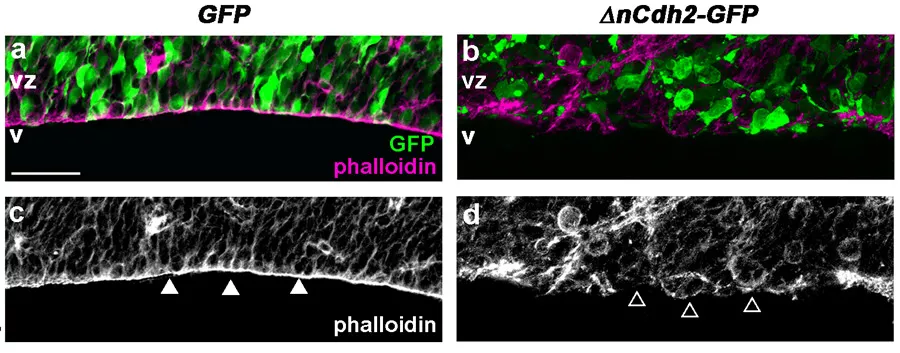
Az adherens kapcsolatok (lilával jelölve) lebomlása a domináns negatív N-cadherin (zöld GFP markerrel jelölve) elektroporálása után (b és d panel) a csak GFP elektroporálásához képest (a és c panel).
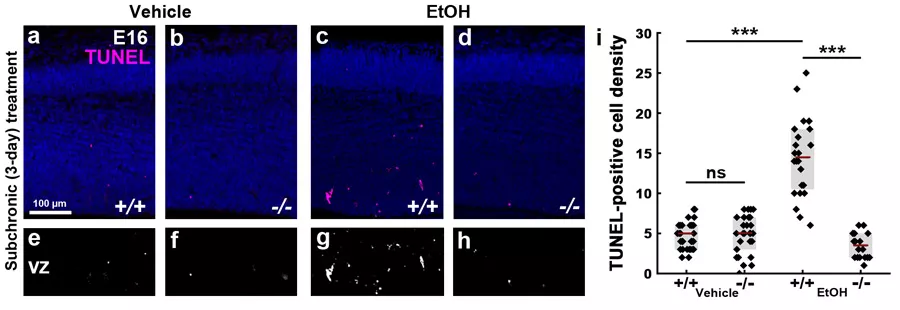
Az anyai alkoholfogyasztás megnövekedett sejthalált okoz a vad típusú embriók agyában (a és c panel). Ezzel szemben az ABHD4 génkiütött állatokban (d panel) ez a növedés nem látható), ami bizonyítja, hogy az ABHD4 jelenléte szükséges a sejthalálszint emelkedéséhez.
A teljes tanulmány angol nyelven a nature.com-on érhető el.